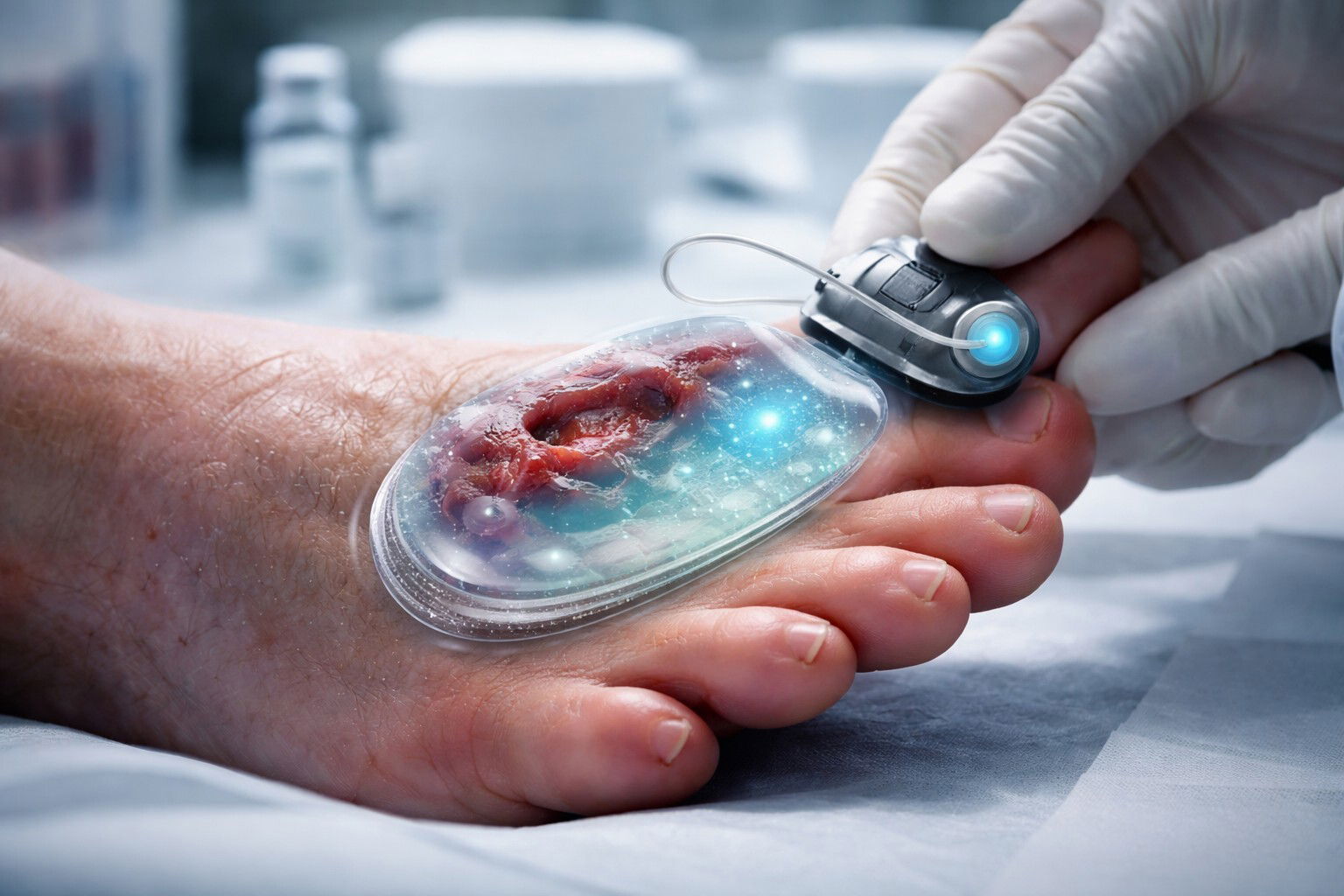
La ricerca di un vaccino universale capace di proteggere l'organismo da minacce infettive di natura diversa rappresenta da decenni uno dei grandi obiettivi della medicina moderna. Ora, un gruppo di ricercatori della Stanford Medicine ha compiuto un passo significativo verso questa meta, sviluppando un vaccino sperimentale somministrato per via intranasale che, nei modelli murini, ha dimostrato di offrire protezione simultanea contro virus respiratori, batteri patogeni e persino allergeni comuni. Il lavoro, pubblicato il 19 febbraio sulla rivista Science, apre prospettive inedite per la prevenzione delle malattie respiratorie, superando i limiti della vaccinologia tradizionale basata sulla specificità antigenica.
La strategia sviluppata dal gruppo guidato da Bali Pulendran, professore di microbiologia e immunologia presso Stanford, si discosta radicalmente dai principi che hanno dominato la vaccinologia fin dai tempi di Edward Jenner. Invece di presentare al sistema immunitario un frammento riconoscibile del patogeno – come la proteina spike del SARS-CoV-2 – questo approccio innovativo mima i segnali di comunicazione che le cellule immunitarie si scambiano durante un'infezione reale. Il risultato è l'integrazione coordinata dei due principali sistemi di difesa dell'organismo: l'immunità innata e quella adattativa.
Il limite principale dei vaccini convenzionali risiede nella rapida evoluzione dei patogeni. Quando virus come l'influenza o il SARS-CoV-2 modificano le strutture presenti sulla loro superficie, i vaccini esistenti possono perdere efficacia, rendendo necessari aggiornamenti annuali o richiami periodici. Come spiega Pulendran, "è sempre più evidente che molti patogeni sono in grado di mutare rapidamente. Come il proverbiale leopardo che cambia le sue macchie, un virus può alterare gli antigeni sulla sua superficie". Questa caratteristica ha reso finora impraticabile l'idea di un singolo vaccino efficace contro famiglie virali diverse o addirittura contro categorie di patogeni non correlate tra loro.
La chiave del nuovo approccio sta nell'attivazione prolungata del sistema immunitario innato. Tradizionalmente, questo sistema risponde entro minuti dall'infezione con una difesa ad ampio spettro, mobilitando cellule dendritiche, neutrofili e macrofagi, ma la sua azione si esaurisce normalmente nel giro di pochi giorni. Il sistema adattativo, invece, produce anticorpi e linfociti T specializzati che mantengono memoria dell'infezione per anni, ma richiede settimane per svilupparsi completamente. Il vaccino sperimentale riesce a mantenere attivo il sistema innato per mesi, creando uno stato di allerta persistente nei polmoni.
Questa strategia trae origine da osservazioni precedenti sul vaccino antitubercolare Bacillus Calmette-Guerin, somministrato annualmente a circa 100 milioni di neonati in tutto il mondo. Alcuni studi avevano suggerito che questo vaccino potesse ridurre la mortalità infantile causata da infezioni diverse dalla tubercolosi, ma il meccanismo rimaneva oscuro. Nel 2023, il gruppo di Pulendran aveva chiarito nei modelli murini come questa protezione incrociata funzionasse: i linfociti T richiamati nei polmoni dalla risposta adattativa continuavano a inviare segnali che mantenevano attive le cellule dell'immunità innata per mesi, invece dei soliti giorni.
Il team ha identificato questi segnali come citochine che attivano i recettori toll-like sulle cellule immunitarie innate. Partendo da questa scoperta, i ricercatori hanno progettato una formulazione sintetica – attualmente denominata GLA-3M-052-LS+OVA – che replica questi segnali dei linfociti T. Il vaccino include anche un antigene innocuo, l'ovalbumina (OVA), una proteina dell'uovo che attira i linfociti T nei polmoni e contribuisce a sostenere la risposta innata potenziata per settimane o mesi.
Negli esperimenti pubblicati su Science, i topi hanno ricevuto il vaccino sotto forma di gocce nasali, alcune cavie con dosi multiple a distanza di una settimana. Dopo la vaccinazione, ciascun animale è stato esposto a un virus respiratorio. Con tre dosi, i topi sono rimasti protetti dal SARS-CoV-2 e da altri coronavirus per almeno tre mesi. I topi non vaccinati hanno manifestato grave perdita di peso – segno clinico di malattia – e spesso sono morti, con i polmoni che mostravano estesa infiammazione e alti livelli virali. Al contrario, i topi vaccinati hanno perso molto meno peso, sono sopravvissuti tutti e i loro polmoni contenevano quantità minime di virus.
Pulendran descrive l'effetto come un "doppio colpo". La risposta innata sostenuta ha ridotto i livelli virali nei polmoni di un fattore 700. Qualsiasi virus che superasse questa prima barriera veniva rapidamente affrontato da una risposta adattativa accelerata. Il sistema immunitario polmonare diventa così pronto e allerta da poter lanciare le tipiche risposte adattative – linfociti T virus-specifici e anticorpi – in appena tre giorni, un intervallo di tempo straordinariamente breve, spiega il ricercatore. Normalmente, in un topo non vaccinato, questo processo richiede due settimane.
I risultati ottenuti contro i virus hanno spinto il gruppo a testare il vaccino anche contro batteri respiratori patogeni, inclusi Staphylococcus aureus e Acinetobacter baumannii, responsabili di comuni infezioni nosocomiali. Anche in questo caso, i topi vaccinati sono risultati protetti per circa tre mesi. Successivamente, i ricercatori hanno verificato l'efficacia contro gli allergeni, esponendo i topi a una proteina degli acari della polvere domestica, causa comune di asma allergica. Le reazioni allergiche coinvolgono una risposta immunitaria di tipo Th2. I topi non vaccinati hanno sviluppato una forte risposta Th2 con accumulo di muco nelle vie respiratorie, mentre quelli vaccinati hanno mostrato una risposta Th2 molto più debole e vie aeree libere.
Il passaggio successivo è rappresentato dalla sperimentazione umana, a partire da un trial clinico di Fase I per valutare la sicurezza. Se i risultati saranno positivi, seguiranno studi più ampi, potenzialmente includendo esposizioni controllate a infezioni. Pulendran stima che per le persone potrebbero essere sufficienti due dosi somministrate mediante spray nasale. Con finanziamenti adeguati, ritiene che un vaccino respiratorio universale potrebbe diventare disponibile entro cinque-sette anni. Una tale innovazione potrebbe rafforzare le difese contro future pandemie e semplificare la vaccinazione stagionale, consentendo di proteggere con un singolo spray nasale autunnale da COVID-19, influenza, virus respiratorio sinciziale, raffreddore comune, polmoniti batteriche e allergeni primaverili precoci.
Lo studio, condotto con il primo autore Haibo Zhang, ricercatore post-dottorato nel laboratorio di Pulendran, ha coinvolto scienziati della Emory University School of Medicine, della University of North Carolina a Chapel Hill, della Utah State University e della University of Arizona. Il finanziamento è stato fornito dai National Institutes of Health (grant AI167966), oltre che da fondi privati. Resta da verificare se l'efficacia dimostrata nei modelli murini possa tradursi in protezione analoga nell'uomo, considerando le differenze tra i sistemi immunitari delle due specie. Tuttavia, la possibilità di superare il paradigma dell'antigene specifico, dominante da oltre due secoli, rappresenta una prospettiva rivoluzionaria nella prevenzione delle malattie infettive respiratorie.