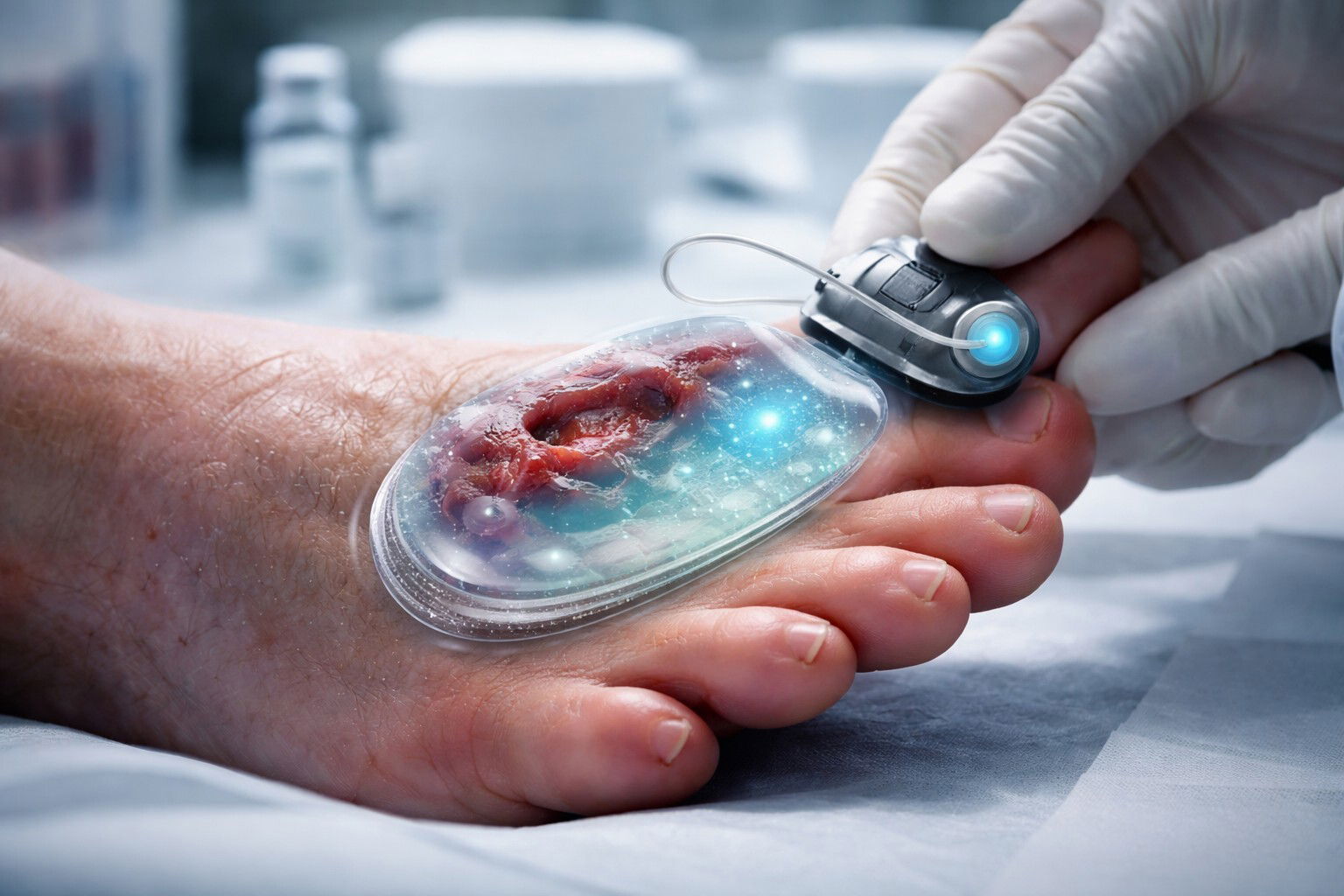
I vasi sanguigni umani rappresentano una delle architetture biologiche più complesse del nostro organismo: si ramificano, si restringono in stenosi che limitano il flusso, si dilatano in aneurismi improvvisi, creando geometrie che influenzano profondamente il movimento del sangue e lo sviluppo di patologie vascolari. Eppure, per decenni, i modelli di laboratorio hanno trattato questi condotti vitali come semplici tubi rettilinei e uniformi, perdendo elementi cruciali per comprendere dove e come insorgono molte malattie cardiovascolari. Un gruppo di ricerca del Department of Biomedical Engineering della Texas A&M University ha ora sviluppato un sistema innovativo di vessel-chip personalizzabili che supera queste limitazioni, aprendo prospettive inedite per lo studio realistico delle patologie vascolari e la valutazione di nuovi farmaci.
I vessel-chip sono dispositivi microfluidici progettati per replicare i vasi sanguigni umani su scala microscopica, offrendo una piattaforma sperimentale alternativa ai modelli animali e adattabile alle caratteristiche di singoli pazienti. Jennifer Lee, studentessa di master in ingegneria biomedica, ha lavorato nel laboratorio del professor Abhishek Jain per progettare un sistema avanzato capace di riprodurre l'intera gamma di morfologie vascolari osservabili nell'organismo umano. Come spiega la ricercatrice, le diverse configurazioni anatomiche alterano significativamente i pattern di flusso sanguigno e lo shear stress che agisce sulla parete interna dei vasi, fattori determinanti nell'evoluzione delle patologie cardiovascolari.
Il lavoro si inserisce in un filone di ricerca portato avanti nel Bioinspired Translational Microsystems Laboratory, dove pochi anni prima il dottor Tanmay Mathur aveva sviluppato un design di vessel-chip rettilinee. La nuova generazione di dispositivi, descritta sulla rivista Lab on a Chip e destinata alla copertina del numero di maggio 2025, rappresenta un salto qualitativo nella complessità strutturale riproducibile. Secondo Jain, professore associato e Barbara and Ralph Cox '53 faculty fellow in ingegneria biomedica, questa piattaforma consente per la prima volta di studiare le malattie vascolari in condizioni che replicano fedelmente i siti anatomici dove queste tendono effettivamente a svilupparsi.
La chiave dell'innovazione risiede nella capacità di integrare materiale cellulare e tessutale vivo all'interno di queste strutture complesse. Attualmente il modello include cellule endoteliali, che costituiscono il rivestimento interno dei vasi sanguigni, ma le versioni future incorporeranno ulteriori tipi cellulari per simulare l'interazione tra diversi tessuti e il sangue in movimento. Questa progressione verso quella che Jain definisce "la quarta dimensionalità degli organi-su-chip" rappresenta una nuova direzione nel campo della biomedicina sperimentale, concentrandosi non solo sulle cellule e sul flusso separatamente, ma sulla loro interazione in stati architettonici complessi che rispecchiano la realtà fisiologica.
Il percorso di Lee illustra efficacemente come il sistema universitario americano favorisca la continuità tra formazione undergraduate e ricerca avanzata. Entrata nel laboratorio mentre era ancora studentessa undergraduate alla ricerca di esperienza pratica, con scarsa familiarità con le tecnologie organ-on-a-chip, ha progressivamente sviluppato un interesse per il potenziale impatto di questo campo sulla ricerca medica futura. Il programma fast-track per il Master of Science le ha permesso di trasformare un progetto esplorativo in una ricerca ad alto impatto pubblicata su una rivista peer-reviewed di rilievo internazionale.
L'approccio metodologico del gruppo di ricerca texano si distingue per l'attenzione alla personalizzazione: i vessel-chip possono essere modellati sulle caratteristiche vascolari individuali, aprendo la strada a una medicina di precisione che testa terapie su modelli specifici del paziente prima dell'applicazione clinica. Questa capacità di riprodurre non solo la geometria generale ma anche le peculiarità anatomiche individuali rappresenta un vantaggio significativo rispetto ai modelli animali, che presentano differenze strutturali e fisiologiche sostanziali rispetto all'uomo.
Le prossime fasi della ricerca punteranno ad aumentare ulteriormente la complessità biologica dei modelli, integrando componenti tissutali aggiuntive che permettano di studiare fenomeni patologici multifattoriali come l'aterosclerosi, le trombosi e le complicanze vascolari del diabete. L'obiettivo a lungo termine è creare piattaforme sperimentali che non solo replicino l'anatomia ma anche la fisiologia dinamica dei vasi sanguigni, consentendo di osservare in tempo reale come diverse condizioni di flusso e stress meccanico influenzino l'espressione genica delle cellule endoteliali e la progressione della malattia.