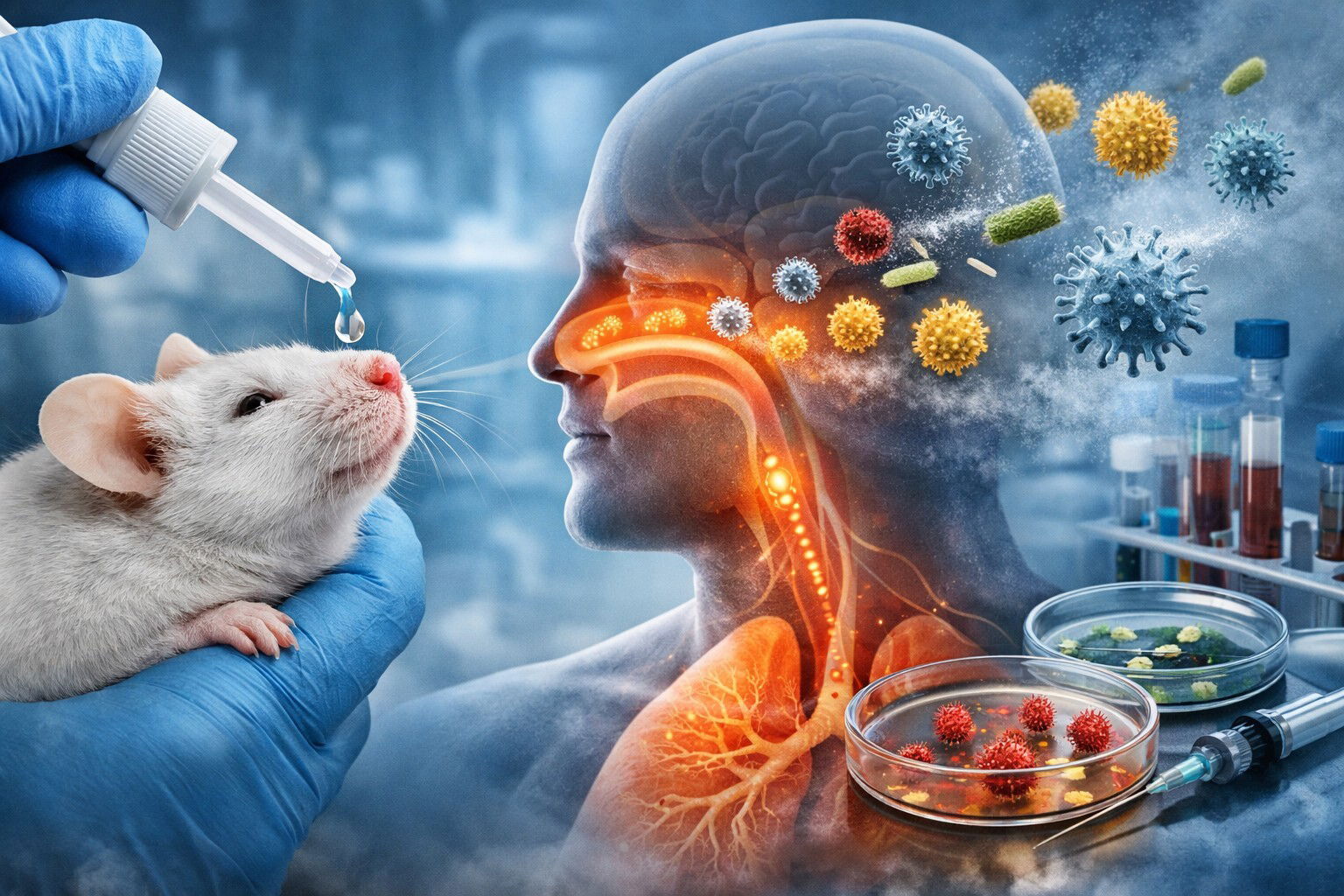
Nella ricerca oncologica contemporanea, l'immunoterapia e i trattamenti a bersaglio molecolare hanno dominato la scena nell'ultimo decennio, ma un filone di ricerca distinto e affascinante sta guadagnando credibilità scientifica: l'utilizzo di batteri ingegnerizzati per colpire selettivamente i tumori solidi dall'interno. Un gruppo di ricercatori dell'Università di Waterloo, in Canada, ha sviluppato un approccio basato sulla biologia sintetica che sfrutta una caratteristica intrinseca di molti tumori solidi — la loro zona centrale priva di ossigeno — per trasformarla da rifugio del cancro in punto vulnerabile. La strategia, ancora in fase pre-clinica, apre prospettive interessanti per quei tumori che resistono alle terapie convenzionali proprio perché le loro cellule ipossiche sono difficilmente raggiungibili da farmaci o radiazioni.
Al centro di questo approccio vi è Clostridium sporogenes, un batterio anaerobio obbligato comunemente presente nel suolo, capace di sopravvivere esclusivamente in ambienti privi di ossigeno. Il nucleo centrale dei tumori solidi è composto da cellule necrotiche e presenta una pressione parziale di ossigeno estremamente bassa, creando le condizioni ideali per la proliferazione di questo microrganismo. Come ha spiegato il professor Marc Aucoin, docente di ingegneria chimica all'Università di Waterloo, "le spore batteriche penetrano nel tumore, trovando un ambiente ricco di nutrienti e privo di ossigeno, che è proprio quello che questo organismo preferisce, e iniziano a consumare quei nutrienti moltiplicandosi. In questo modo colonizziamo lo spazio centrale del tumore e il batterio contribuisce a eliminarlo dall'organismo."
Il meccanismo sfrutta dunque una proprietà biologica già nota — l'anaerobiosi obbligata di Clostridium sporogenes — senza richiedere alcuna manipolazione iniziale del microambiente tumorale. Tuttavia, il gruppo di Waterloo ha dovuto affrontare un ostacolo significativo: quando i batteri si espandono verso le regioni periferiche del tumore, dove piccole quantità di ossigeno sono presenti, iniziano a morire prima di riuscire a eliminare completamente la massa cancerosa. Questo limite intrinseco rischiava di rendere la terapia parzialmente efficace, lasciando vive le cellule tumorali più esterne e ossigenate — spesso le più proliferative.
Per superare questo problema, il team ha inserito nel genoma di Clostridium sporogenes un gene proveniente da un batterio affine con maggiore tolleranza all'ossigeno. Questa modifica genetica consente ai microbi ingegnerizzati di sopravvivere più a lungo nelle zone di confine del tumore. Tuttavia, attivare questa resistenza all'ossigeno in modo permanente e indiscriminato avrebbe comportato un rischio inaccettabile: i batteri avrebbero potuto proliferare nel torrente sanguigno o in tessuti sani, con potenziali conseguenze tossiche gravi per il paziente.
La soluzione a questo problema di controllo è venuta dall'applicazione di un fenomeno naturale batterico noto come quorum sensing, ovvero la comunicazione chimica tra cellule microbiche basata sulla densità della popolazione. I batteri rilasciano continuamente piccole molecole segnale nell'ambiente circostante; quando la loro concentrazione supera una soglia critica — indice che la colonia ha raggiunto una dimensione sufficientemente elevata — viene attivata una risposta genica coordinata. Nel sistema progettato a Waterloo, il gene di tolleranza all'ossigeno si attiva soltanto quando la popolazione batterica all'interno del tumore è abbastanza numerosa da garantire che l'azione si svolga nel microambiente ipossico desiderato, e non in circolo o in altri tessuti.
Questa architettura di controllo rappresenta uno degli aspetti più originali del progetto dal punto di vista della biologia sintetica. Come ha descritto Brian Ingalls, professore di matematica applicata all'Università di Waterloo, il team ha costruito veri e propri circuiti a DNA in cui ogni segmento genico svolge una funzione precisa, analoga a quella di un componente elettronico. La verificabilità e la prevedibilità del sistema sono state testate in uno studio preliminare, nel quale i batteri sono stati programmati per produrre una proteina fluorescente verde come segnale reporter, confermando che il meccanismo di quorum sensing si attivava esattamente al momento previsto e nella quantità attesa.
La traiettoria scientifica di questo progetto si articola in due fasi di ricerca distinte ma complementari. In un primo studio il gruppo ha dimostrato la fattibilità della modifica genetica di Clostridium sporogenes per incrementarne la resistenza all'ossigeno. Nel secondo lavoro, di follow-up, è stato validato il sistema di controllo basato sul quorum sensing tramite l'esperimento con la proteina fluorescente. Il passo successivo, attualmente in programma, consiste nell'integrare entrambi i componenti — il gene di tolleranza all'ossigeno e il circuito di quorum sensing — in un unico ceppo batterico e testarne l'efficacia su modelli tumorali in studi pre-clinici.
Il progetto è nato dal lavoro del dottorando Bahram Zargar, co-fondatore del Center for Research on Environmental Microbiology (CREM Co Labs), una società con sede a Toronto che collabora attivamente con il gruppo di Waterloo. La supervisione accademica è stata condivisa tra Ingalls e il professor Pu Chen, ora in pensione, già titolare di ingegneria chimica a Waterloo. Un contributo determinante è stato portato anche da Sara Sadr, ex dottoranda dell'ateneo canadese, che ha avuto un ruolo di primo piano nell'avanzamento della ricerca. L'iniziativa incarna l'approccio interdisciplinare dell'Università di Waterloo, che unisce ingegneria chimica, matematica applicata e scienze della vita per tradurre scoperte fondamentali in potenziali soluzioni mediche concrete.
Restano aperte numerose questioni scientifiche prima che questa strategia possa approdare alla sperimentazione clinica sull'uomo. Sarà necessario dimostrare che il sistema integrato si comporta in modo sicuro e controllabile in modelli animali, verificare l'assenza di effetti fuori bersaglio e valutare la risposta immunitaria dell'ospite nei confronti del batterio ingegnerizzato. La ricerca sulla batteriologia anti-tumorale ha una storia che risale agli studi pioneristici del XIX secolo, ma solo con gli strumenti della biologia sintetica moderna è oggi possibile progettare livelli di controllo e precisione che rendono questi approcci realisticamente valutabili in contesti clinici.